氨基酸分子的特点
同学们早上好
萍姐给你讲化学
今天我们学习蛋白质的性质
同学们对蛋白质应该比较熟悉吧,蛋白质是生物体内一类极为重要的功能高分子化合物,是生命活动的主要物质基础
几乎一切的生命活动过程都与蛋白质有关,没有蛋白质就没有生命。氨基酸是组成蛋白质的基本结构单位,我们要认识蛋白质,必须先认识氨基酸
氨基酸
羧基分子烃基上氢原子被氨基取代的化合物称为氨基酸,氨基酸分子中含有氨基和羧基
组成蛋白质的氨基酸几乎都是a氨基酸,就是氨基和羧基连在同一个碳原子上
常见的氨基酸有甘氨酸、谷氨酸、丙氨酸、苯丙氨酸
天然氨基酸均为无色晶体,熔点较高,在200-300°C熔化时分解,它们能溶于强酸和强碱溶液。除少数外一般都溶于水,二难溶于乙醇、乙醚。
氨基的性质
两性
既能与盐酸反应(氨基显碱性)有能与氢氧化钠反应(羧基显酸性)
2、成肽反应
在酸和碱存在的条件下加热,通过一分子的氨基与另一分子的羧基间脱水一份子水,缩合形成肽键(-CO NH -)称为成肽反应
蛋白质的结构与性质
蛋白质是一类非常重要的含氮生成物物高分子化合物,有C、H、O、S等元素组成,有些蛋白质含有P,少量蛋白质含有微量Fe、Cu、Zn、Mn。人体内所具有的蛋白质种类达到10万种以上
蛋白质最显著的特征是独特和稳定的结构
性质
1、两性
2、水解在酸碱或者酶的作用下,水解生成相对分子量较小的肽类化合物,最终水解得到氨基酸氨基酸被肠壁吸收进入血液,再在人体内重新合成人体所需要的蛋白质
3、盐析
少量的盐(如硫酸铵、硫酸钠、氯化钠等轻金属盐)能促进蛋白质的溶解,当蛋白质溶液中加入的盐溶液能达到一定浓度时,反而使蛋白质的溶解度降低而从溶液中析出,这种作用称为盐析。盐析是可逆的,再加入水可以重新使蛋白质溶解,采用多次盐析和溶解可以分离蛋白质
4、变性
在某些物理和化学因素的影响下,蛋白质的理化性质和生理功能发生改变的现象称为蛋白质的变性,物理因素包括:加热、加压、搅拌、振荡、在外线照射,超声波等
化学因素包括:强酸、强碱、重金属、三氯乙酸、丙酮等
同学们医院用酒精消毒,紫外线照射,都是蛋白质的变性,目的是杀死蛋白质
另外如果我们重金属中毒,缓解的话可以喝牛奶和豆浆,再去医院
5、颜色反应
蛋白质溶液中加入浓硝酸会有白色沉淀产生,加热沉淀会变黄色。含有苯环的蛋白质均能发生这个反应
皮肤指甲不慎粘上浓硝酸也会出现黄色就是这个缘故
我在给学生上课做实验总也不慎沾到过浓硝酸,手非常疼,黄色要一段时间才能退去
同学们今天的知识你了解了吗?有任何疑问可以私聊萍姐,萍姐会为你一一解答
同学们明天见
《中国大百科全书(第2版)》读书笔记01197-氨基酸
氨基酸 amino acid
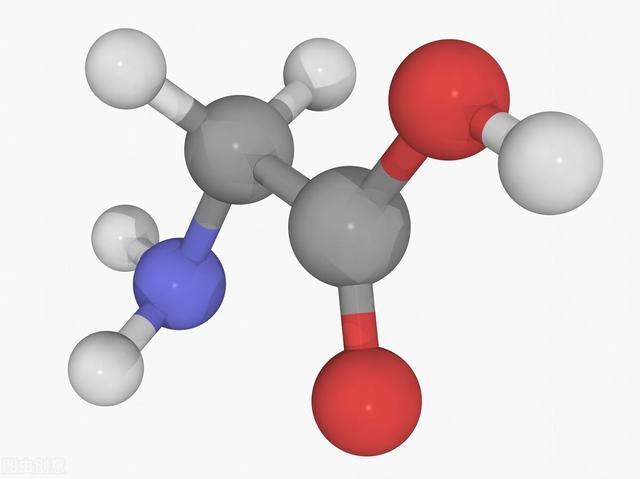
甘氨酸分子模型
一类既含氨基又含酸性基团的有机化合物。已发现的氨基酸、亚氨基酸有700余种,其中绝大多数是L-型的α-氨基酸。构成蛋白质的常见的氨基酸有20种,严格地说19种氨基酸和1种亚氨基酸是构成蛋白质所必需的。
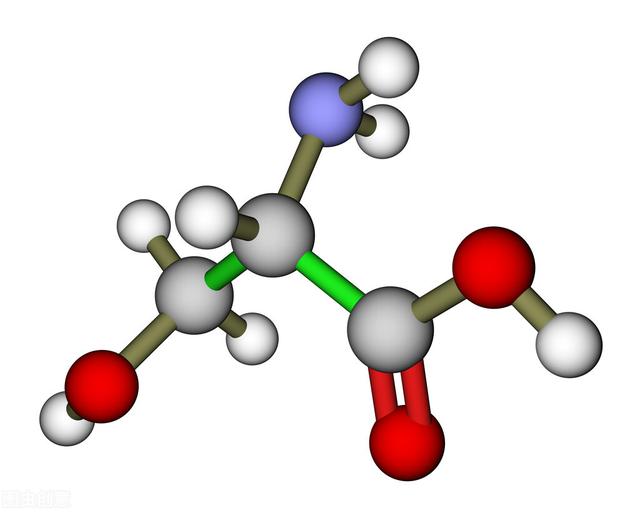
丝氨酸分子模型
α氨基酸的结构如图所示。在同一个碳原子上同时接有氨基、羧基、氢原子和一个侧链基团(R)。最简单的氨基酸是甘氨酸(Gly),它的侧链基团都是氢原子。其他含有脂肪族侧链基团的有丙氨酸(Ala)、缬氨酸(Val)、亮氨酸(Leu)、异亮氨酸(Ile);侧链含有脂肪族羟基的有丝氨酸(Ser)和苏氨酸(Thr);侧链含有芳香族基团的有苯丙氨酸(Phe)、酪氨酸(Tyr)和色氨酸(Trp);组氨酸(His)的侧链为咪唑基团。除了上述的中性氨基酸外,还有在中性环境带有正电荷的赖氨酸(Lys)和精氨酸(Arg)两种碱性氨基酸;谷氨酸(Glu)和天冬氨酸(Asp)是两种酸性氨基酸。后两种酸性氨基酸的侧链羧基为酰胺所代替时各成为谷氨酰胺(Gln)和天冬酰胺(Asn)。此外还有两个含硫的氨基酸,半胱氨酸(Cys)和甲硫氨酸(Met)。除Gly外,α-氨基酸都有两种异构体,分别称L型和D型。存在于蛋白质中的氨基酸都是L型。脯氨酸(Pro)是一个环亚氨基酸,它的结构见图中的(2)。此外,在蛋白质中还有很罕见的硒代半胱氨酸和吡咯赖氨酸。
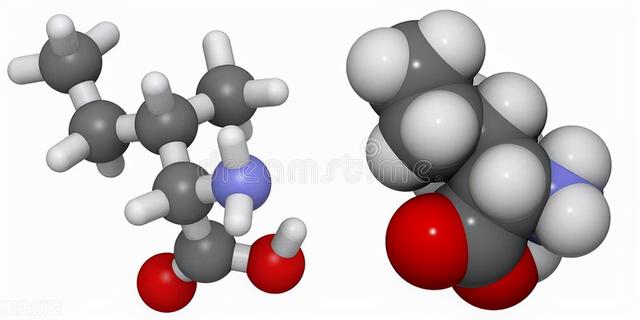
异亮氨酸分子模型
蛋白质中的这些氨基酸均是由三联体核苷酸编码的。在蛋白质分子成熟过程中,有不少氨基酸的侧链经过酶的作用转变成它们的衍生物。这是蛋白质翻译后加工的一个重要内容。
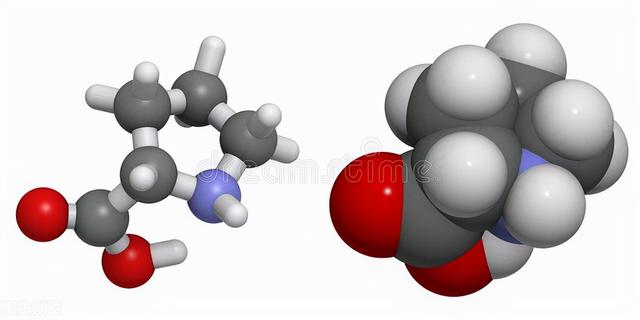
脯氨酸分子模型
有些氨基酸,动物自身不能合成而必须从食物中获得,缺乏这些氨基酸会导致营养不良。这类氨基酸被称为必需氨基酸。对人体来说,必需氨基酸包括:Val、Leu、Ile、Thr、Phe、Trp、Lys和Met。而Arg和His仅是婴儿必需的,需适量补充。
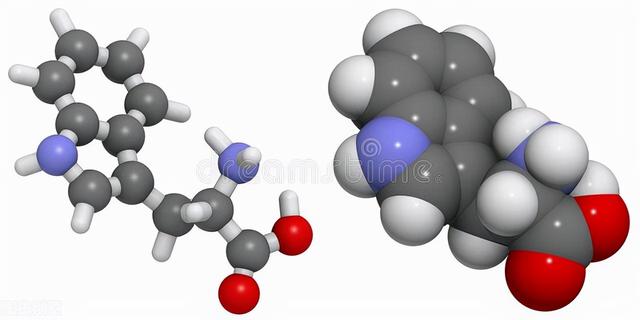
色氨酸分子模型
α-氨基酸具有多种多样的性质。最主要的有两种。一是它们的氨基和羧基都能电离,可成为兼性离子。二是它们同时具有亲水-疏水性质。此外,它们形成α-螺旋和β折叠链的倾向也各不相同;它们的侧链R的大小也有很大差别;分子中的一些带负电性的原子还能形成氢键。这些性质对于蛋白质的结构和功能均产生很大的影响。
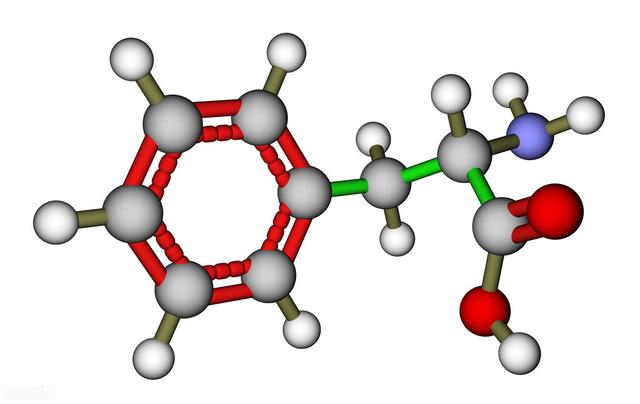
苯丙氨酸分子模型
除了参与蛋白质形成的常见的20种氨基酸外,在机体中还有其他多种多样的氨基酸。如高等动物代谢中间产物鸟氨酸和瓜氨酸,起激素作用的甲状腺素(即碘代酪氨酸),以及作为神经递质的γ氨基丁酸等。植物中也有许多种游离氨基酸,其功能多数尚不详。
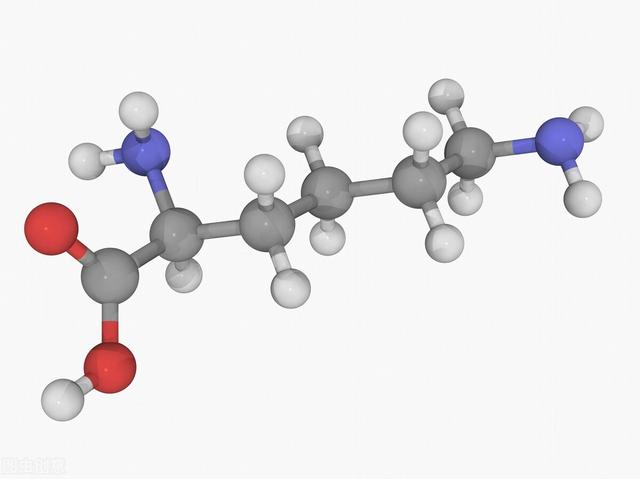
赖氨酸分子模型
氨基酸不仅是机体中构成蛋白质的必不可少的组分,还是合成肽的原料和重要的试剂。还可用作调味剂、食物添加剂和药物。谷氨酸钠盐,即味精,世界年产量在30万吨左右。Gly可作甜味剂。许多种氨基酸的混合液是重要的急救药,用于补液。个别氨基酸也可药用。
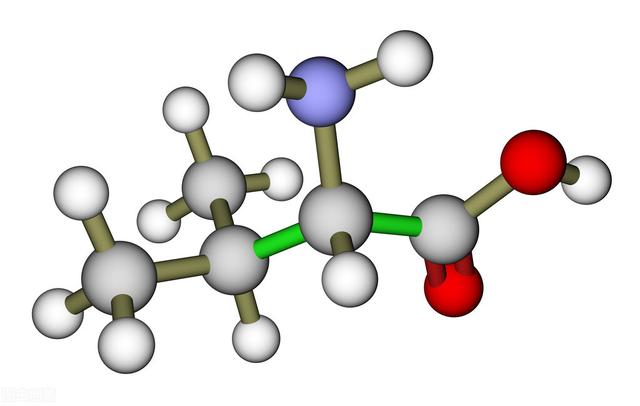
缬氨酸分子模型
生产氨基酸的主要方法是发酵法,几乎找到了生产所有蛋白质中所含氨基酸的发酵菌。如L-Glu、L-Lys、L-Arg等都可以用发酵法生产。利用酶的专一性,可将其底物转变成相应的氨基酸糖。例如天冬氨酸酶可以将富马酸转变成L-Asp。微生物发酵法价格低廉,但是酶法的产物容易提纯。

天冬氨酸分子模型
摘自:《中国大百科全书(第2版)》第1册,中国大百科全书出版社,2009年
《中国大百科全书(第2版)》读书笔记01197-氨基酸
学习打卡第一天:
医学生集合了[大笑]
生物化学与分子生物学:蛋白质主要由碳、氢、氧、氮、硫组成,有些蛋白质还含有少量磷或金属元素铁、铜、锌、锰、钴、钼,个别还含有碘。各种蛋白质的含氮量很接近,平均为16%。
氨基酸根据其侧链的结构和理化性质可分为五类:非极性脂肪族氨基酸、极性中性氨基酸、芳香族氨基酸、酸性氨基酸、碱性氨基酸。非极性脂肪族氨基酸:甘氨酸、丙氨酸、缬氨酸、亮氨酸、异亮氨酸、脯氨酸、甲硫氨酸;极性中性氨基酸:丝氨酸、半胱氨酸、天冬酰胺、谷氨酰胺、苏氨酸;含芳香环的氨基酸:苯丙氨酸、酪氨酸、色氨酸;酸性氨基酸:天门冬氨酸、谷氨酸、;碱性氨基酸;精氨酸、赖氨酸、组氨酸。
在某一PH的溶液中,氨基酸解离成阳离子和阴离子的趋势及程度相等,成为兼性离子,呈电中性,此时溶液的PH称为该氨基酸的等电点。
含共轭双键的氨基酸具有紫外线吸收性质。
茚三酮反应是指茚三酮水合物在弱酸性溶液中与氨基酸共加热时,氨基酸被氧化脱氨、脱羧,而茚三酮水合物被还原,其还原物可与氨基酸加热分解产生的氨结合,再与另一份子茚三酮缩合成为蓝紫色化合物,此化合物最大吸收峰在570nm波长处。由于此吸收峰值的大小与氨基酸释放出来的氨量成正比,因此可作为氨基酸定量分析方法。
由2-20个氨基酸相连成的肽成为寡肽,而更多的氨基酸相连成的肽称为多肽。多肽链有两端,其游离a-氨基的一端称为氨基末端或N-端,游离a-羧基的一端称为羧基末端或C-端。肽链中的氨基酸分子因脱水缩合而基团不全,成为氨基酸残基。[奋斗][奋斗]


 添加微信免费咨询
添加微信免费咨询
