荧光氨基酸
绿色荧光蛋白的来历
荧光蛋白的发现与应用
文/ Serina
生命的颜色
在海洋中,栖息着一类美丽而神奇的生物——水母。水母是一类古老的水生无脊椎软体动物。多数水母拥有颜色绚丽的伞性身躯及自体发光的能力,可散发出点点淡蓝色荧光,与摇曳的海水相映成辉,常引人无限遐想。没有人知道水母发光的能力是如何进化而来的,这些美丽的海洋精灵遍布在世界各地的海洋中,如繁星般点缀着浩瀚的海底世界。千百万年来,这些美丽的水母如光明的使者,出现在诗人、画家和摄影师的作品中,为人类艺术史增添了一抹亮色。
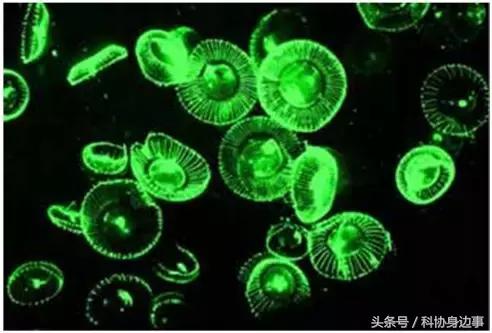
▲Aequorea Victoria水母
直至20世纪中期,一位日本科学家下村修才注意到并着手研究了水母这一独特的发光现象,并发现其荧光源自一种会发光的蛋白——水母蛋白,它可以发出蓝色的荧光并将其传递给另一种绿色荧光蛋白,最终使水母产生绿色的荧光。随后马丁·查尔菲及钱永健两位科学家对GFP加以改造和利用,并正式将其成功引入整个生命科学领域,引发了一场生命科学领域细胞及蛋白研究技术的巨大革命。至今为止,利用改造后的荧光蛋白标记活体细胞的方法已在世界各实验室得到广泛推广,而下村修、马丁·查尔菲及钱永健三人也因为他们做出的巨大贡献共同获得了2008年诺贝尔化学奖。下面,我们将逐步介绍水母素、绿色荧光蛋白与人类科学共同发展的辉煌历史。

▲2008年,瑞典皇家科学院将当年诺贝尔化学奖分别授予日本科学家下村修(左一)、美国科学家马丁·查尔
水母蛋白的发现故事
下村修是最早研究这种水母发光现象的科学家之一。20世纪50年代,他所在的伍兹霍尔海洋生物实验室正致力于研究生物的发光现象。1955—1961年间,下修村已经对水萤火虫(Cypridina)体内的发光机制进行了深入研究,并发现这种小生物的发光需借助于其体内一种奇特的蛋白,并将其命名为荧光素酶。遗憾的是,下修村发现仅靠荧光素酶自身并不足以发光——很多年以后人们才发现荧光素酶本身没有发光能力,但其可以催化一种叫做荧光素的小分子化合物并使其发光——但这项研究令他意识到很多海洋生物的发光能力可能依赖于其体内产生的某种发光蛋白。因此,他转而研究更多的海洋生物,以寻找其他具有发光能力的蛋白。
后来,在其导师约翰森的建议之下,他最终决定将工作重点放在研究一种名为Aequorea victoria的水母身上。为此他和约翰森多次驱车到达华盛顿大学的星期五港实验室打捞大量水母,并将它们分批带回位于马萨诸塞州的实验室进行蛋白提取实验。先前关于荧光素酶的研究为下村修提供了大量研究经验,他很快发现在水母伞性区域的边缘聚集有大量能够发光的发光细胞,并从中分离出了一种可以发光的蛋白,并将其称作“水母蛋白”。该研究刊登在1962年《细胞和比较生理学杂志》上。
据称有一天,下村修又提取了一份不能发光“失败”的蛋白样品,下班前随手将其倒入水池中,并关好实验室的灯准备回家。临走前他例行环视了实验室一周后准备锁门,下一刻他惊奇地发现水池中竟散发着蓝色的荧光!他立刻断定可能是水池中的某种成分激活了水母蛋白的发光能力。在此后的几天,他对水池中可能存在的所有离子及化学组分进行了逐一筛查,并最终发现钙离子可以激活水母蛋白发光能力。
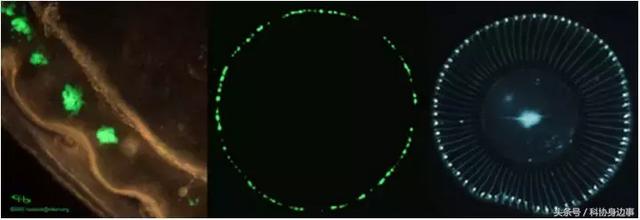
▲水母发光细胞在Aequorea Victoria水母中的形态。左图为水母发光细胞的显微图片。中图为Aequorea Victoria水母在黑暗中的颜色。右图为Aequorea Victoria水母在可见光中的颜色。
1963年,下村修和约翰森等在《科学》上报道了这一神奇的蛋白结合钙离子后发光的独特机制。原来在未结合钙离子时,水母蛋白可与一种名为腔肠素的小分子之间共价结合。当钙离子存在时,每个水母蛋白可与两个钙离子结合,并通过氧化反应使蛋白与腔肠素之间的共价键断裂,形成游离的腔肠素及CO2。由腔肠素负责发光,该反应是迅速而短暂的。自然光会削弱钙离子与水母蛋白之间的结合能力,并最终使水母蛋白重新回到不结合钙离子、但与腔肠素共价结合的状态。
在自然界中,Aequorea Victoria水母在受到惊吓时可迅速发出光芒,而数分钟后光芒则自行消退,即是这一有趣生化反应的宏观体现。
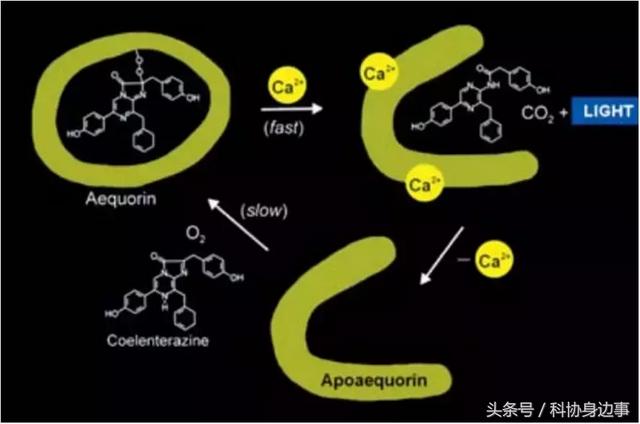
▲水母蛋白结合钙离子后发光的分子机制。图片摘自下村修获得诺贝尔化学奖后在诺贝尔讲座所做的研究报告
在其后的研究中,阿什利和里奇韦解析了该蛋白的编码基因,并将其表达于其它生物体中,以监测生物体内钙离子浓度的动态变化。钙离子是生物体中一类重要的信号分子,因此这项技术使人们首次成功观察到活体内钙离子浓度变化的情况。在数十年后的今天,这项技术仍是科研人员测定活体内钙离子的主流方法之一。如2010年,武治长井实验室在《公共科学图书馆·综合》期刊上曾利用表达水母蛋白的动物细胞观察其体内钙离子的浓度变化情况。
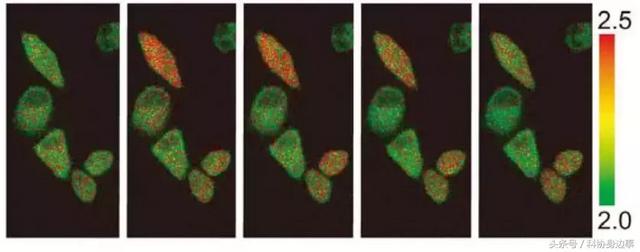
▲体外培养的的动物细胞,在转入水母荧光蛋白后于显微镜下呈现的钙离子浓度热图。图中红色代表细胞内钙离
绿色荧光蛋白横空出世
水母蛋白的发现与改造为体内钙离子浓度的测定带来重大的技术突破。但水母为生命科学领域做出的贡献却远不止于此。
下村修在研究水母荧光蛋白时,发现高纯度的水母荧光蛋白在加入钙离子后可发出蓝色的荧光,但在黑暗中水母及水母的发光细胞都呈现绿色。这是一个有趣的科学现象,下村修为此感到既新奇、又困惑。经过一系列预实验,他推测在水母中很可能还存在另外一种蛋白,可以对水母荧光蛋白的发光特性造成一定影响。他继续优化蛋白提取工艺,并最终证实在水母发光细胞中,确实还存在一种小分子蛋白。但这种蛋白的含量极其微弱,以至于他们无法对它的化学性质进行分析。在漫长的10年后,他终于获取了足够量的此种蛋白,并通过一系列实验获得了该蛋白的晶体结构。对蛋白晶体的研究结果显示,这种蛋白本身不具有发光能力,但能吸收水母荧光蛋白发出的蓝色光波,并将其转化为绿色的光波放出。他将该蛋白命名为“绿色荧光蛋白”。这一出色的成果最终发表在1979年的《美国科学院院刊》中。
但遗憾的是,当时的研究者们并没有意识到绿色荧光蛋白的应用前景。一晃20年过去了,一位在英国剑桥大学做博士后工作的马丁·查尔菲博士偶然注意到了下村修的工作。当时马丁·查尔菲正在研究一种名为秀丽隐杆线虫的小型模式动物的神经元发育情况。这种小蠕虫仅有1.5mm长,通体透明,是观察神经细胞发育及迁徙的绝佳模式动物。但马丁·查尔菲在显微镜下跟踪神经细胞发育情况时,他发现在层层叠叠的细胞组织中跟踪神经细胞的标记情况仍具有一定困难。在得知绿色荧光蛋白的性质后,他意识到自己或许可以将绿色荧光蛋白表达在秀丽隐杆线虫的神经细胞中,并以此标记需要观察的细胞,使它们在层层叠叠的透明组织中“脱颖而出”。从1992—1994年的2年间,他一直致力于在体外克隆绿色荧光蛋白的编码基因,并先后将其成功表达在了原核模式生物大肠杆菌及秀丽隐杆线虫中,并最终获得了带有绿色荧光蛋白标记的神经元的转基因秀丽隐杆线虫。在荧光显微镜下,这些线虫经蓝色激发光照射后会发射出绿色的荧光,清晰地展示了神经细胞的位置及结构,非常美丽。
这项开拓性的工作发表在当年的《科学》杂志上。文章发表后,众多科学家开始意识到可以利用绿色荧光蛋白对一些观察困难的细胞、亚细胞器或蛋白进行活体成像分析。经过十余年的发展,利用绿色荧光蛋白进行活体标记的技术已被细胞学研究领域广泛采用,并成为一项经久不衰的经典实验技术。

▲带有GFP标记的秀丽隐杆线虫神经元结构。如图所示依次为秀丽隐杆线虫的头部神经节、背神经索、腹神经索
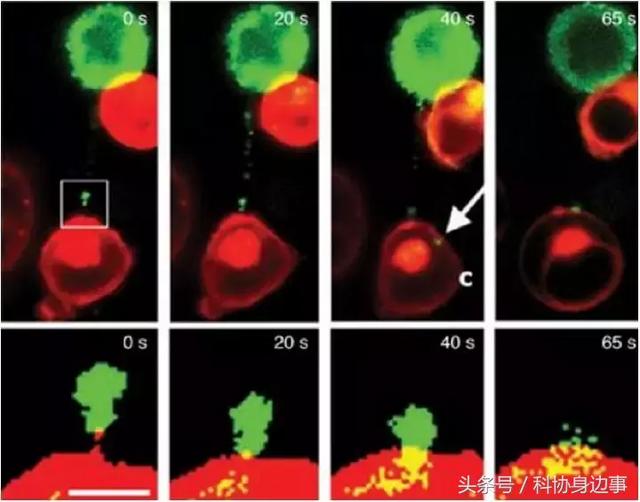
▲利用绿色荧光标记的目标蛋白在荧光显微镜下进行移动的时间轨迹。如图,上一排为带有绿色荧光标记的目标蛋
随着绿色荧光蛋白标记技术的蓬勃发展,科研人员逐渐发现单纯的绿色荧光蛋白常常不能完全满足实验者的研究需要,有很多科研人员希望在实验中同时标记两种以上的细胞或蛋白,以研究它们之间的相互作用情况。针对这种需求,时任加州大学圣迭戈分校药理学教授以及化学与生物化学教授的钱永健博士开始着手改造并寻找绿色荧光蛋白的变体。钱永健带领的科研团队研究了绿色荧光蛋白的结构特点,并对其重要氨基酸位点进行了突变或置换,最终获得了一系列绿色荧光蛋白的变种蛋白。有的较绿色荧光蛋白荧光更强、有的经激发后可发出黄色、蓝色、青色及红色荧光,为此后的科学研究提供了极大的便利。而钱永健本人也因这一突出贡献与下村修和马丁·查尔菲分享了2008年的诺贝尔化学奖。
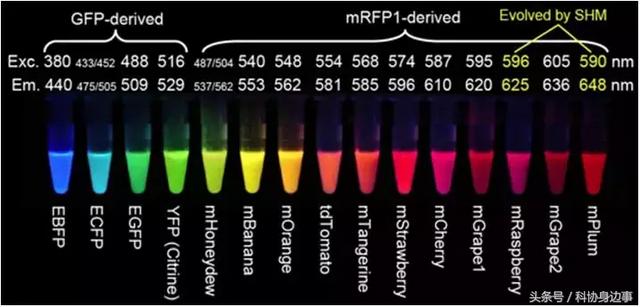
▲钱永健实验室改造的一系列荧光蛋白变体及其被激发光照射后呈现出的颜色
在无数科学家们的努力下,蛰居于水母内的水母蛋白及绿色荧光蛋白已经被导入病毒、放线菌、酵母、植物、果蝇、线虫、小鼠、大鼠、人类细胞等几乎所有的模式生物,为无数科学研究乃至人类重大疾病的研究做出了巨大的贡献。荧光蛋白发出的生命之光,将继续照亮生命科学领域未来的道路。
来源:今日科协微信公众号
中国科协各级组织要坚持为科技工作者服务、为创新驱动发展服务、为提高全民科学素质服务、为党和政府科学决策服务的职责定位,推动开放型、枢纽型、平台型科协组织建设。接长手臂,扎根基层,团结引领广大科技工作者积极进军科技创新,组织开展创新争先行动,促进科技繁荣发展,促进科学普及和推广,真正成为党领导下团结联系广大科技工作者的人民团体,成为科技创新的重要力量。——习近平
前沿科技解读丨生命的颜色——荧光蛋白的发现与应用,绿色荧光蛋白的来历


 添加微信免费咨询
添加微信免费咨询
